

 更多“某药物在一定温度下分解的速率常数与温度的关系为 k的单位是h…”相关的问题
更多“某药物在一定温度下分解的速率常数与温度的关系为 k的单位是h…”相关的问题
NO与Cl2进行反应:2NO(g)+Cl2(g)====2NOCl(g),在一定温度下,反应物浓度和反应速率的关系如下:
| c(NO)/(mol·L-1) | c(Cl2)/(mol·L-1) | υ/(mol·L-1·s-1) |
| 0.50 1.00 1.00 | 0.50 0.50 1.00 | 1.14 4.56 9.12 |
求反应级数及在该温度下的速率常数k。
某温度下,反应
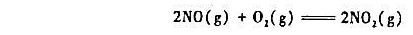
的速率常数k=8.8×10-2dm6·mol-2·s-1。已知此反应对O2是1级的,当两种反应物浓度都是 0.050mol-1·dm-3时,此反应的反应速率是多少?
某温度下反应2NO(g)+O2(g)====2NO2(g)的速率常数k=8.8×10-2dm6·mol-2·s-1,已知反应对O2来说是一级反应,则对NO为______级,速率方程为______;当反应物浓度都是0.05mol·dm-3时,反应的速率是______。
气相反应4A→Y+6Z的反应速率常数kA与温度的关系为: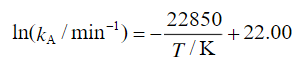 ,且反应速率与产物浓度无关。求:
,且反应速率与产物浓度无关。求:
A.若溶液中溶剂在某浓度区间遵从拉乌尔定律,则在该浓度区间组分B必遵从亨利定律
B.温度越高、压力越低,亨利定律越正确
C.因为亨利定律是稀溶液定律,所以任何溶质在稀溶液范围内都遵守亨利定律
D.温度一定时,在一定体积的溶液中溶解的气体体积与该气体的分压力无关力越低,亨利定律越正确
A.升高温度
B.降低温度
C.增大产物的浓度
D.加入催化剂
A.-12℃
B.-3℃
C.3℃
D.12℃