

 更多“298.15K时,参考单质的标准摩尔熵为零。()”相关的问题
更多“298.15K时,参考单质的标准摩尔熵为零。()”相关的问题
A.117.0kJ·mol-1
B.58.5kJ·mol-1
C.-58.5kJ·mol-1
D.-117.0kJ·mol-1
若参加化学反应的各物质的摩尔定压热容可表示为
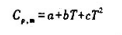
试推导化学反应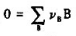 的标准摩尔反应熵
的标准摩尔反应熵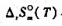 与温度T的函数关系式,并说明积分常数
与温度T的函数关系式,并说明积分常数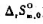 如何确定.
如何确定.
平衡常数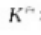 将(),反应的标准摩尔吉布斯自由能变将()。
将(),反应的标准摩尔吉布斯自由能变将()。
25℃和标准状态下,N2和H2反应生成lgNH2(g)时放出2.71kJ的热量,则(NH3,g,298.15K)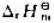 等于()kJ·mol-1.
等于()kJ·mol-1.
A.-2.71/17
B.2.71/17
C.-2.71×17
D.2.71×17